玛巴洛沙韦(Xofluza)是Cap依赖型核酸内切酶抑制剂(Cap-dependent endonuclease inhibitor),也是目前唯一一款获批用于治疗流感的单剂量口服药物,为美国FDA近20年来首次批准的具有新型作用机制的抗流感病毒药物。目前已在包括美国、日本、中国在内的多个国家获批。
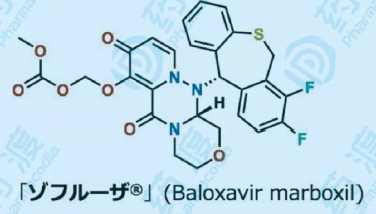
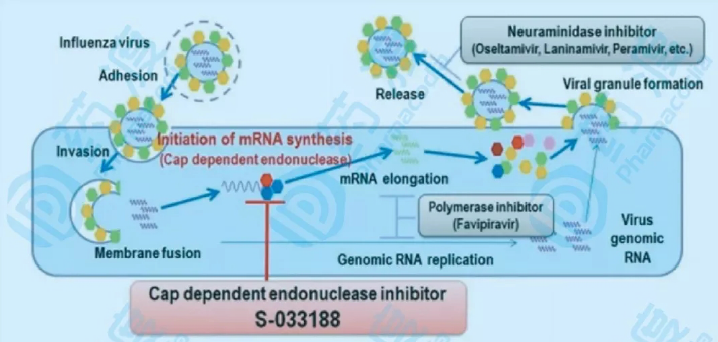
南京知和创新药研究院开发的LHZH基于巴洛沙韦分子,在对抗病毒耐药性和提升抗病毒活性方面进行了针对性设计。同时,具有广谱抗流感的特性,对甲、乙型流感病毒、高致死禽流感病毒等均具有非常优越的活性,并预期具有更加优异的口服生物利用度,无食物效应问题,进一步提高了安全有效性;且不受48小时内服药黄金期的限制,在症状出现72小时后服药仍然有效,也不易受到流感病毒变异的影响而产生抗药性。具备了第二代巴洛沙韦的主要特征。
目前,在研或已上市的抗流感PA抑制剂,专利期均较长,短期内没有仿制的可能 。南京知和开发的LHZH项目已申请专利(专利号:202111291506.9),具有独立知识产权,不受相关专利的限制 。

巴洛沙韦酯是前药,在体内水解为巴洛沙韦而发挥作用。培优科学家运用AI技术,在深入研究其构效关系基础上,借助变分自编码器与强化学习组合的深度学习、机器学习,进行了靶点验证和活性筛选工作,深入研究Cap依赖型核酸内切酶结构学和生理生化学特征,对基础研究数据进行识别、分类、提取、分析,准确预测“药物-靶点”相互作用关系,优化设计的具有me-better潜质候选化合物。
根据对标化合物构效关系的深入研究,保留了其发挥抗流感作用至关重要的结构特征,从两个方面引入分别具有对抗病毒变异和增强抗病毒活性作用的结构片段,因而在关键非临床对比研究中表现优异,完全达到设计目标:不受48小时服药时间的限制,且不易产生抗药性,具备了第二代巴洛沙韦的特征,在某种程度上可称之为加强版的第二代玛巴洛沙韦。
成熟度与风险分析
LHZH设计思路中的HBJ策略已有进入二期临床的候选药,研究结果令人鼓舞;XI引入策略化合物也获临床默示许可。两策略并行实施不仅会大大增强候选药优势,成功把握度也将进一步得到保障,项目风险极低,具有极高开发前景。
本项目化合物LHZH在避开已有专利的同时也形成了自己的专利。已同知识产权专家进行多次推演讨论,并委托国家知识产权局专利检索咨询中心检索专利相关化合物,检索结果表明未检出相关公开结构,这说明本发明化合物在新颖性、创造性和实用性方面均可满足专利授权条件;已开展的体内外药效等多项关键性研究表明其效果显著。
同时,LHZH合成步骤比巴洛沙韦减少6步,手性中心减少,生产周期和成本将大大降低,在即将到来的DRGs付费模式下,将比已上市或在研同靶点化合物更具整体竞争优势。